Klinikum Rheine
Alles für Ihre medizinische Versorgung
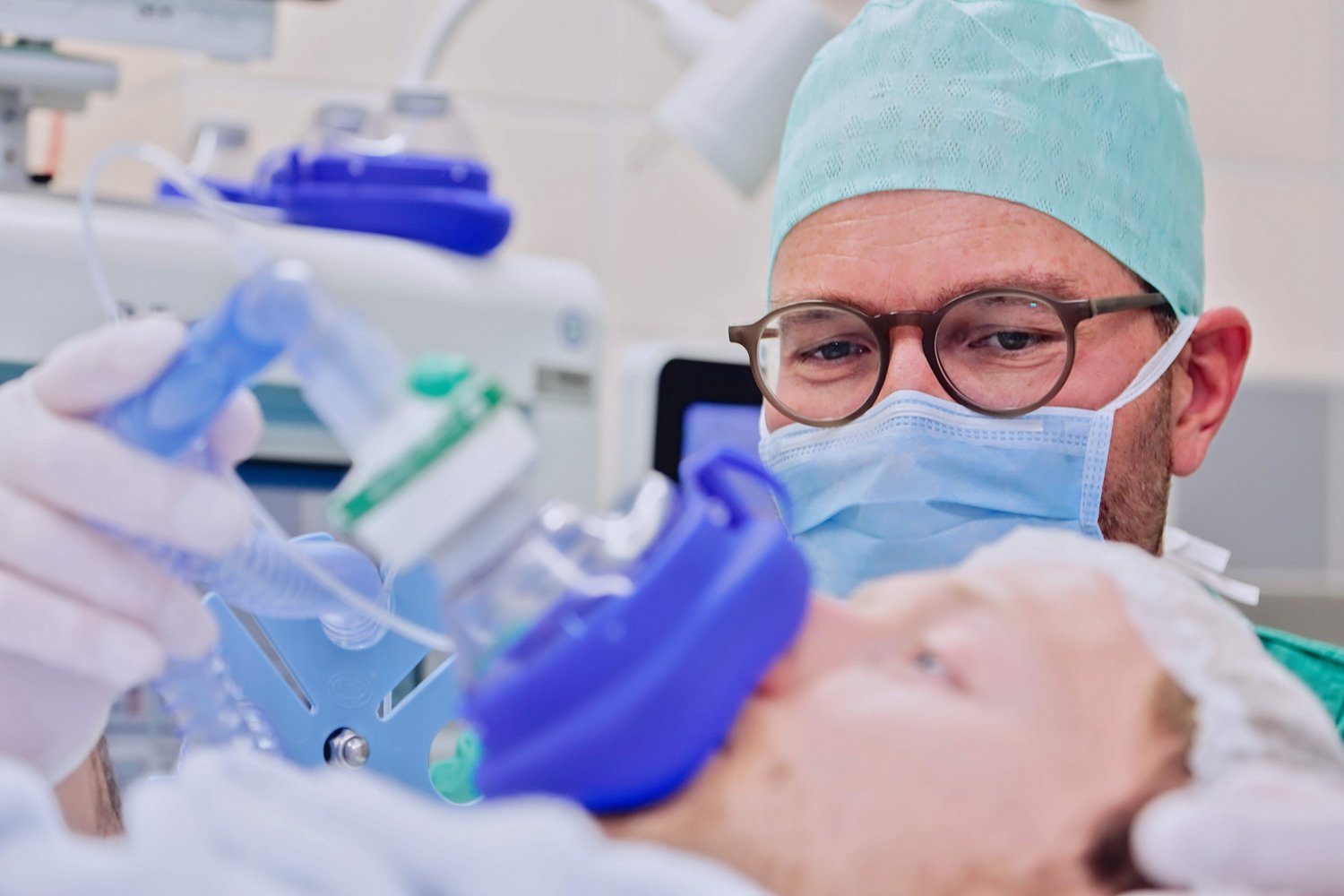
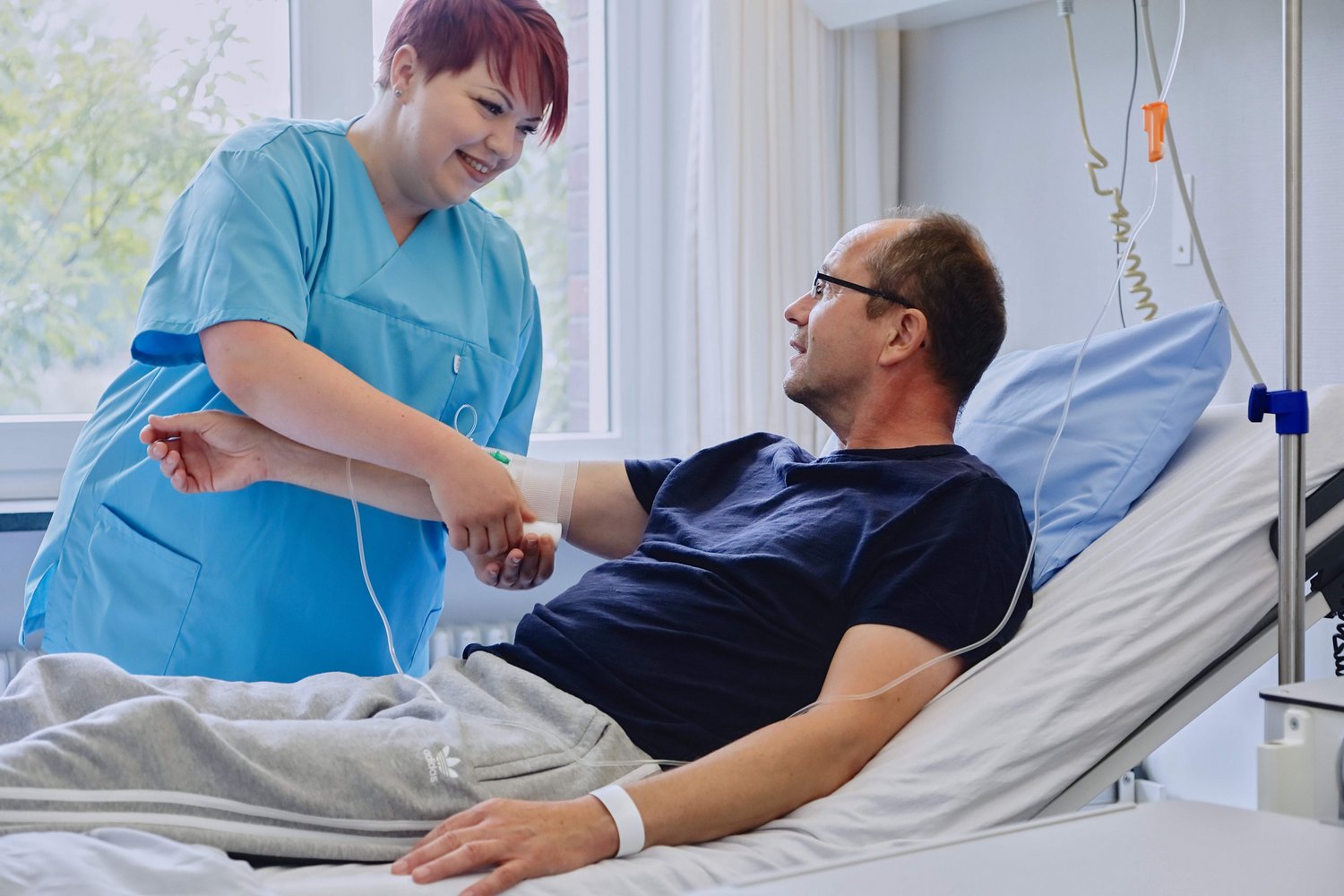
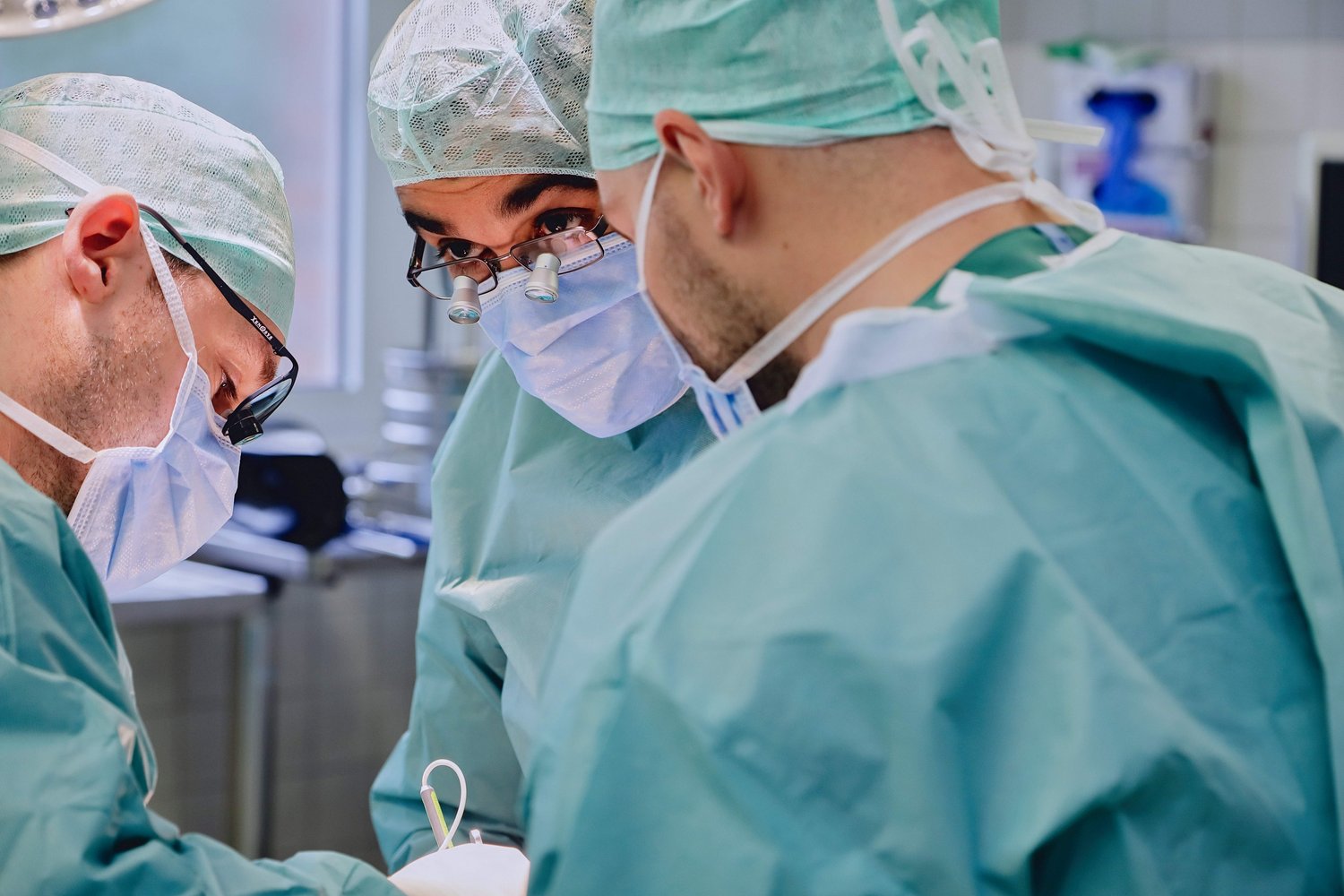
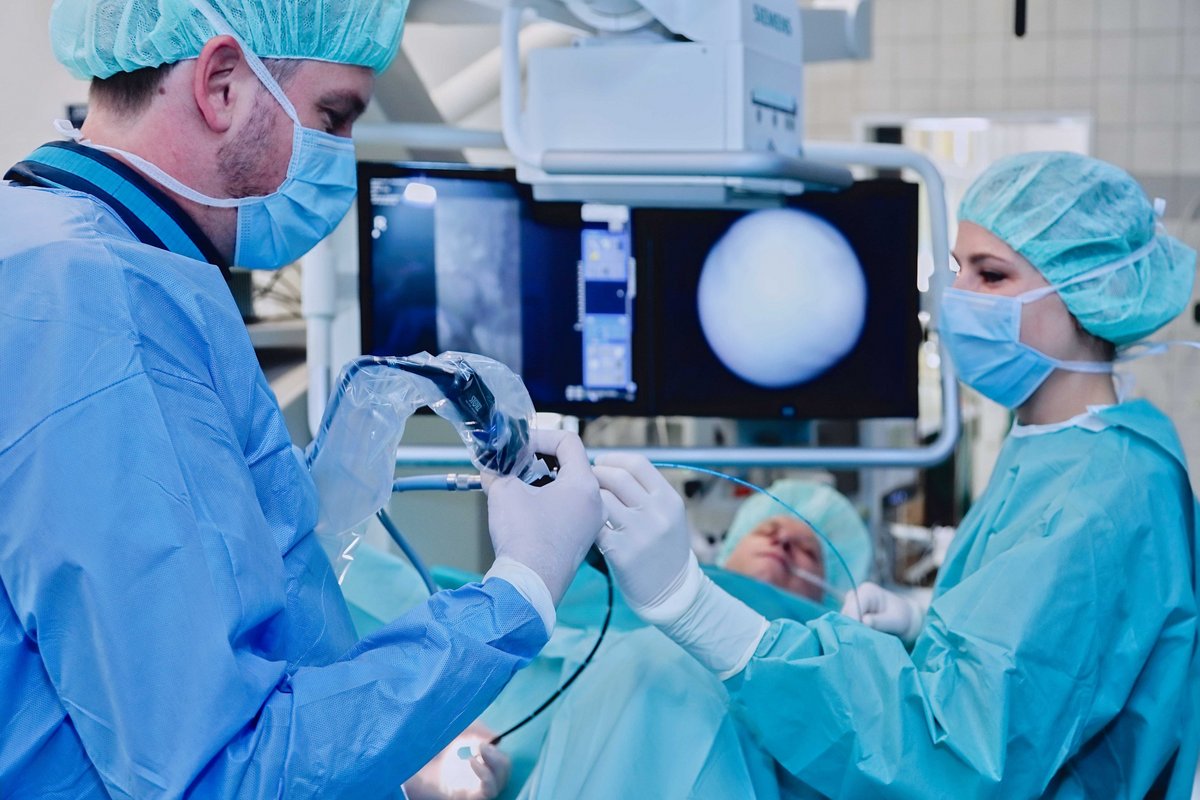
Als Akutkrankenhaus stehen wir den Menschen in Rheine und Umgebung 24 Stunden am Tag und 365 Tage im Jahr zur Seite. Das Klinikum besteht aus 2 Betriebsstätten - dem Mathias-Spital und dem Jakobi-Krankenhaus. Mit dem breiten medizinischen Gesamtspektrum können wir zahlreiche Erkrankungen und Beschwerden behandeln.
Weitere Angebote
Sie benötigen weitere Unterstützung?

Wir bieten Ihnen abseits der medizinischen Fachbereiche weitere Angebote für eine ganzheitliche Gesundheitsversorgung. Und auch darüber hinaus bieten wir Ihnen unsere Unterstützung an, um den Wechsel von Krankenhaus ins eigene Zuhause sorgenfrei zu meistern.
Kontakt
Mathias-Spital
Wo Sie uns finden
Mathias-Spital
Klinikum Rheine
Frankenburgstraße 31
48431 Rheine
Kontakt
Jakobi-Krankenhaus
Wo Sie uns finden
Jakobi-Krankenhaus
Klinikum Rheine
Hörstkamp 12
48431 Rheine
Terminkalender
Veranstaltungen in der Mathias-Stiftung
Fortbildungsveranstaltung des Uroonkologischen Zentrums Klinikum Ibbenbüren
Anlässlich der Erstzertifizierung als Uroonkologisches Zentrum ist Fachpublikum aus der Urologie herzlich zur Fortbildungsveranstaltung des Uroonkologischen Zentrums Klinikum Ibbenbüren eingeladen.
Sport und Krebs - das macht Sinn!
Die Veranstaltung klärt darüber auf, warum Sport für Krebspatient:innen sinnvoll ist und welche Möglichkeiten es gibt.
Girls' & Boys' Day
Jährlicher Informationstag für Schüler:innen, der Einblicke in die Ausbildungsberufe der Mathias-Stiftung gibt.
Für Menschen da
Weitere Tätigkeitsfelder der Mathias-Stiftung
Karriere
Ein Teil des Ganzen
Entdecken Sie Ihre beruflichen Möglichkeiten innerhalb des Klinikum Rheine oder auch innerhalb der Mathias-Stiftung mit ihren vielseitigen Einrichtungen und Leistungsbereichen. Als eine der größten Arbeitgeber in der Region bieten wir nicht nur einen zukunftssicheren Arbeitsplatz, sondern auch die Chance, einen sinnstiftenden Beitrag für das große Ganze zu leisten.
Jetzt einsteigen


Gesundheit im Verbund
Die Mathias-Stiftung
Die Mathias-Stiftung verfolgt ausschließlich und unmittelbar christliche, gemeinnützige und mildtätige Zwecke zur Förderung und Durchführung von Tätigkeiten der Caritas, der Alten- und der Gesundheitspflege. Als einer der größten Arbeitgeber im Bereich der stationären und ambulanten Gesundheits- und Pflegedienstleistungen im nördlichen Münsterland, versorgen über 4.400 Mitarbeitende hilfsbedürftige Menschen. Mit insgesamt drei Akutkrankenhäusern, einer Rehabilitationsklinik, sechs Alten- und Pflegeinrichtungen, medizinischen Versorgungszentren, ambulanten Pflegedienst, eine eigenen Bildungseinrichtung sowie einer eigenen Servicegesellschaft beweisen wir ganzheitliche Gesundheitsversorgung aus einer Hand.
Meldeportal